Физико-химические свойства озона
Основные физические и химические свойства озона. Сравнение свойств кислорода и озона в газообразном и жидком состоянии. Периоды полураспада озона в воде и воздухе.
Что такое озон
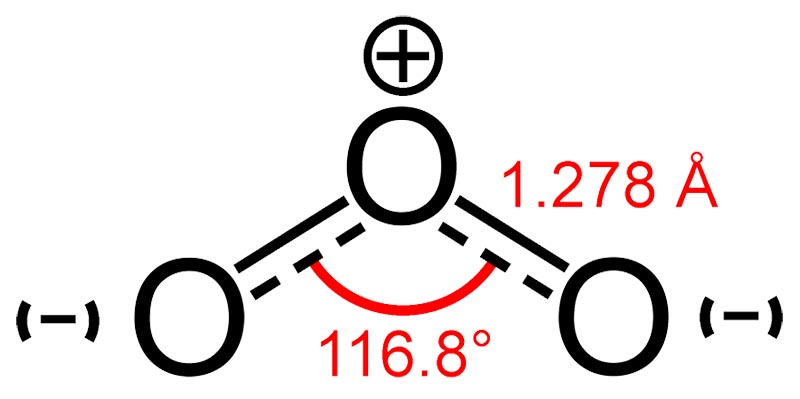
ОЗОН О₃ (от греч. ozon-пахнущий). Озон – это аллотропная модификация кислорода, состоящая не из двух атомов кислорода, как «обычный» кислород, а из трех. Плотность газообразного озона по кислороду 1,5, по воздуху 1,62. Ниже температуры кипения озон — темно-синяя жидкость, плотность 1,71 г/см3 (при — 183°С).
Озон — один из наиболее сильных окислителей (гораздо сильнее обычного кислорода). Он окисляет все металлы (за исключением Au и платиновых), а также большинство других элементов (таблица озоностойкости материалов). При действии на некоторые неорганические и органические соединения образует озониды и перекисные соединения. Присутствие озона в газовой смеси можно установить по реакции («Обычный» кислород O2 в реакцию KI не вступает):
O3 + 2KI + H2O = I2 + O2 + 2KOH
Сильные окислительные свойства озона позволяют использовать его при получении многих органических веществ, для отбеливания бумаги, масел и т.д. Озон убивает микроорганизмы, поэтому его применяют для очистки воды и воздуха (озонирование).
Сравнение свойств кислорода и озона
| Свойство | Озон (О₃) | Кислород (О₂) |
| Цвет | Газ: голубой Растворенный в воде: фиолетово-синий при концентрации выше 20 ppm | Газ: бесцветный Растворенный в воде: светло-голубой |
| Молекулярная масса, г/моль | 48 | 32 |
| Температура кипения при 1 атм., оС (К) | – 112 (161,15) | -183 (90,15) |
| Температура плавления при 1 атм., оС (К) | – 192,7 (80,45) | -218,35 (54,8) |
| Плотность газа, кг/м3 | 2,144 | 1,429 |
| Растворимость в воде при 0 °C | 0,64 | 0,049 |
| Электрохимический потенциал, В | 2,08 (гидроксильный радикал ОН° 2,80) | 1,23 |
Прочие свойства озона:
| Свойство | Озон (О₃) |
| Плотность жидкости, г/см3 | 1,59 |
| Плотность твердого озона, г/см3 | 1,73 |
| Поверхностное натяжение при 77,4 К, дин/см | 43,8 |
| Вязкость жидкости при 77,6 К, сПз | 4,17 |
| Теплота испарения при 161,2 К, кДж/моль | 15,19 |
| Теплота плавления, кДж/моль | 2,1 |
| Теплота растворения в воде при 291,15 К, кДж/моль | 14,2 |
| Диэлектрическая постоянная газа | 1,0019 |
| Диэлектрическая постоянная жидкости | 4,79 |
Полураспад молекул озона
Молекула О3 неустойчива и самопроизвольно превращается в O2 с выделением тепла. При небольших концентрациях (без посторонних примесей) озон разлагается медленно. Нагревание и контакт озона с ничтожными количествами органических веществ, некоторых металлов или их окислов резко ускоряет превращение. Наоборот, присутствие небольших количеств HNO3 стабилизирует озон, а в сосудах из стекла, некоторых пластмасс или чистых металлов озон при — 78°С практически не разлагается.
Подробнее про полураспад молекул озона:
Список источников:
- Физическая химия озона: монография / В.В. Лунин, М.П. Попович, С.Н. Ткаченко. – 2-е изд., испр. и доп. – Москва: МАКС Пресс, 2019. – 540 с.
перейти в каталог
Выберите озонатор под ваши задачи: производительность, мобильность, тип генерации
перейти в каталог







